Imprinting genomico: identificati i fattori determinanti
Fino a non molto tempo fa si riteneva che la genetica avrebbe svelato i segreti della vita, poi è arrivata l’epigenetica, che alla decifrazione e interpretazione del codice genetico ha aggiunto le scoperte relative alle modificazioni scritte sulla sequenza del DNA e delle proteine su cui questo è avvolto che possono trasmettersi alle generazioni successive.
Giovanna Grimaldi, dell’Istituto di genetica e biofisica ‘Adriano Buzzati Traverso’ del Consiglio nazionale delle ricerche (Igb-Cnr) di Napoli, è autore insieme ad Andrea Riccio e Paolo Pedone della Seconda Università di Napoli e a Didier Trono dell’Ecole Polytechnique Federale di Losanna di uno studio pioneristico, pubblicato su Molecular Cell, che promuove un modello di integrazione tra codici genetico ed epigenetico.
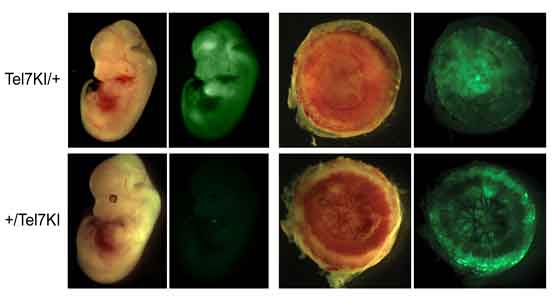
“Questo studio riguarda la regolazione dei cosiddetti geni imprinted: gli unici che, sebbene ereditati da entrambi i genitori, vengono espressi per tutta la vita dell’individuo soltanto dalla copia proveniente da uno dei due, in seguito a modificazioni specifiche del Dna che avvengono durante la maturazione delle cellule sessuali maschili e femminili (gametogenesi) dei genitori stessi”, spiega Giovanna Grimaldi. “L’imprinting genomico è fondamentale nella crescita degli individui e i suoi difetti sono alla base di disordini della crescita, come le sindromi di Beckwith-Wiedemann e di Silver-Russell, e malattie neurologiche, quali le sindromi di Angelman e Prader-Willi. Per tale ragione questa ricerca è stata finanziata anche da Telethon”.
Comprendere i meccanismi che regolano l’imprinting genomico è quindi fondamentale per la salute dell’uomo. “Nei nostri laboratori abbiamo caratterizzato il ruolo di una proteina, Zfp57, che insieme ad altri fattori garantisce la conservazione dei segnali epigenetici dall’embrione all’adulto”, aggiunge Andrea Riccio, che è anche associato presso l’Igb-Cnr. “Poiché i segnali epigenetici sono labili, l’aver scoperto un’intera filiera di proteine in grado di riconoscerli, preservarli e propagarli alla progenie rappresenta un passo avanti fondamentale nella definizione degli elementi che integrano codice genetico ed epigenetico. Contiamo in futuro di valutare se altri fattori affini a Zfp57 svolgano funzioni analoghe e partecipino quindi, come questa proteina, alla scrittura e lettura del codice epigenetico”.
Questo studio aiuta a comprendere come la riprogrammazione epigenetica del Dna sia controllata da fattori genetici: “Ad esempio, in patologie dovute a disordini dell’imprinting genomico potrebbero esserci difetti sia nella proteina Zfp57 sia nella sequenza del Dna cui essa si lega o nelle sue modificazioni epigenetiche”, prosegue Grimaldi. “I segnali epigenetici sono importanti anche per il nostro benessere e stato di salute. Pertanto, la conoscenza di fattori che controllano l’interazione tra la scrittura genetica e quella epigenetica, come Zfp57 e proteine associate, diventa di fondamentale interesse per la comunità scientifica”.
“Questo lavoro sarà di grande impatto”, commenta il direttore dell’Igb-Cnr, Antonio Baldini. “I ricercatori e le ricercatrici del nostro Istituto sono riusciti ad anticipare l’era della ‘Next Generation Sequencing’. Per esplorare il mondo dell’epigenetica sarà fondamentale decifrare non solo il codice genetico ma anche le sue modificazioni ed individuare gli attori di tali eventi. Confidiamo di poter crescere in questa direzione e di non mancare all’appuntamento con questa nuova frontiera della ricerca mondiale”.